介绍
优点特点
产品具备方便快捷、安全性高、灵敏度高、重复性好、稳定性强、特异性高的特点
产品列表
新型冠状病毒(2019-nCoV)核酸检测试剂盒(PCR-荧光探针法–冻干型)
样本类型:包括咽拭子标本,鼻咽拭子标本,肺泡灌洗液和痰标本等类型,适用性更广。
原理:本试剂盒采用实时定量PCR,以新冠病毒SARS-CoV-2的ORF1ab和N基因设计性引物,经实时定量PCR扩增以实现对SARS-CoV-2的核酸检测。
适应场景:在美国CLIA实验室认证或同等性质的非美国地区实验室进行。 操作要求具有一定的专业性,操作人员应经过专业实时定量PCR培训
规格
样本类型:鼻咽或口咽拭子和痰
靶点:SARS-CoV-2 ORF1ab基因、N基因和E基因
检测方法:RT-PCR
阳性一致性:100%
阴性一致性:100%
临时命令#313701
在-25摄氏度至-15摄氏度的温度下储存
需要RNA提取试剂盒(未提供)
每个试剂盒包含:
- 灭菌水;
- ORF1ab/N 反应液;
- 酶混合液;
- 核算扩增反应液;
- 阳性对照;
- 阴性对照
新型冠状病毒、甲型流感病毒和乙型流感病毒核酸检测试剂盒(PCR-荧光探针法–冻干型)
2019- nCoV/IAV/IBV核酸检测试剂盒已经开发出来,用于检测人鼻咽拭子、口咽拭子、痰液、肺泡灌洗液样本中的SARS-CoV-2、甲型流感和乙型流感病毒RNA。
该试剂盒经过CE认证,仅用于体外诊断。
样本类型:定性检测人鼻咽拭子、口咽拭子、痰液、肺泡灌洗液标本中新型冠状病毒、甲型流感病毒(IAV)、乙型流感病毒(IBV)的RNA。
优点:多重检测,同时检测新型冠状、甲型流感、乙型流感病毒核酸
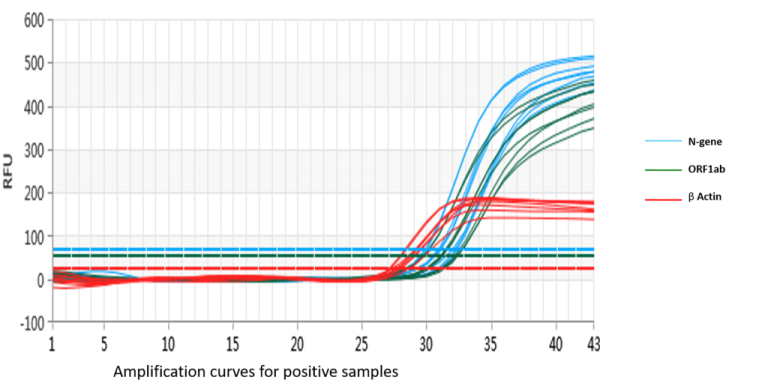
原理
SARS CoV2/IAV/IBV PCR试剂盒是一种一步实时逆转录聚合酶链反应(RT-PCR)诊断试剂盒。用于检测SARS-CoV-2以及甲型和乙型流感。
多重检测使用荧光探针和引物检测SARS-CoV-2核衣壳(N)基因和ORF1ab基因内的三个特定区域。β-球蛋白用于内部控制,以监测样本和提取过程的质量。包括阳性和阴性对照。从患者样本中提取的RNA可直接用于分析,以进行反向转录和定量扩增。用作阳性对照的假病毒颗粒作为提取过程和RT-PCR的对照。
试剂盒组成
组成 | 主要成分 | |
1 | SARS-CoV-2反应混合物,冻干 | 引物、探针、PCR反应缓冲液、dNTPs、酶等。 |
2 | SARS-CoV-2阳性对照,冻干 | 包括ORF1ab和N基因的冻干假病毒颗粒检测目标序列 |
3 | 阴性对照 | 超纯水 |
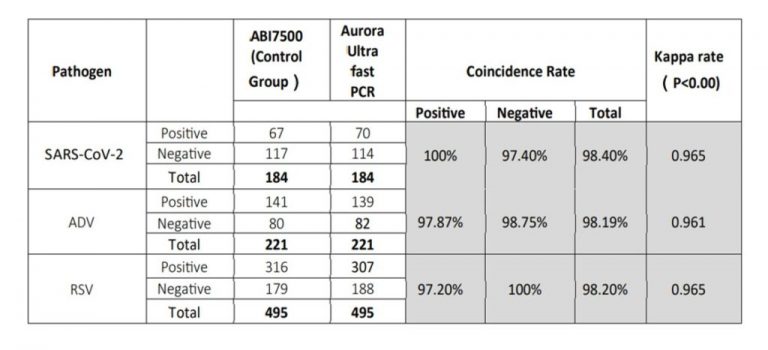
分析特异性
该检测试剂盒可用于检测SARS-CoV2
特别是甲型流感病毒(2009年H1N1、H1N1、H3N2、H5N1、H7N9)和乙型流感病毒(Yamagata, Victoria)。
FAM通道检测SARS-CoV-2,HEX通道检测甲型流感,Cy5通道检测乙型流感,ROX通道检测人类内部参考基因作为质量控制。
检出限
- SARS-CoV2 (2019-nCoV ) : 400 copies/mL.
- 甲型流感病毒:5 TCID50/mL.
- 乙型流感病毒:0 TCID50/mL.
新型冠状病毒2019-nCoV核酸检测试剂盒(荧光PCR法)——加拿大IO授权和欧盟CE认证
更多详情,请浏览英文版介绍页面
新型冠状病毒(SARS-CoV-2)实时多重RT-PCR试剂盒是一种体外诊断测试剂,用于定性检测SARS-CoV-2上呼吸道和下呼吸道标本(包括鼻咽或口咽拭子和痰),符合公共卫生当局推荐的标准。该产品包含用于rRT-PCR的混合物、RT-PCR混合酶和质控品,用于呼吸道标本中新型冠状病毒RNA的体外定性检测。结果可用于对SARS-CoV-2 RNA的鉴定。在感染期间,新型冠状病毒RNA通常可在上下呼吸道标本中检测到。检测结果呈现阳性,提示有新冠病毒感染,但不排除细菌感染或与其他病毒合并感染。所检测到的病原体可能不是导致疾病的确切原因。阳性结果需要按照当地的法规进行报告。阴性结果并不排除新型冠状病毒感染,也不应作为治疗或其他患者管理决策的唯一依据。阴性结果必须结合临床观察、病史和流行病学信息。